作者:陈建林、吴莉红、吴良燕、梁思群、戴娟、沈月单位:柳州市柳铁中心医院案例发生比较典型,为了避免发生类似的问题,梳理原因分析过程并整理实验验证资料,与大家进行分享。
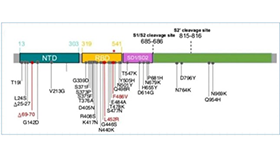
9月21日下午16:00接班时,值班老师称当日新冠核酸RT-PCR扩增失败致使检验报告全部未发,正在准备对标本重新复查。实验室使用的新型冠状病毒(2019-nCoV)试剂盒检测ORF1ab、N基因和RNase P基因。
当天出现异常结果如下:第2-7列样本和A7孔位弱阳性对照扩增曲线未出(正常阴性样本和弱阳性对照内参基因都应有扩增,弱阳性对照ORF1ab和N 基因也应有扩增)(图1),第1列样本内参基因正常检出,E8孔位弱阳性对照正常检出(图2)。
由于时间紧迫,笔者立即参与到原因分析中来。经查当日核酸提取仪、荧光定量PCR仪都运作正常且前一天实验结果未出现此种情形,初步排除了仪器的原因。由于存在少部分样本有扩增曲线而大部分样本扩增失败,(因提取试剂1块96深孔板同时提取16份样本,上机检测使用的8连管体系放置在相邻的两列)从扩增失败样本的分布来看可初步排除提取试剂的质量问题。据检测人员回忆,本次检测所使用的扩增体系存在混用情况,即有扩增曲线的体系为当天分装,不出结果的体系为前一天分装。由于前一天分装体系弱阳性对照不出(A7),第一直觉是前一天分装的扩增体系出现问题。但是,查核前一天分装体系的批号和保存状态与当天一致,并未发现异常。由于质控失控,所有标本需要重新复查。虽然初步排除了提取试剂的质量问题,为了万无一失,实验人员再次重提核酸进行检测。鉴于扩增体系分装的疑点较大,故换人重新分装扩增体系(批号未变)。检测后奇怪的事情再次出现,见下图。第1-5列样本(使用当天第一次分装体系)内参基因均有曲线(图3),第6-7列样本(用当天第二次分装体系)包括弱阳性对照都未有阳性扩增曲线(图4),实验再次失败。难道是同一批号的扩增试剂中有部分存在质量问题?(在此之前出现过一次扩增试剂酶混合液量不足的案例)再次核对试剂的批号、保存状态以及试剂批号更换性能验证结果均未见异常,综合判断此种情形存在的概率非常低。这时再次将疑点转移到试剂的分装上来。为了进一步明确问题所在,笔者对扩增体系进行了第三次分装,同时为了排除一切干扰因素,本次分装弃用之前的方法(体系先混在小容器中,再用排枪快速分装),改用20ul单通道加样枪在试剂盒原管中混合体系进行分装,同时设计对照试验明确原因所在。扩增结果详见图5-图8。本次试验第1-4列和第6列为笔者分装体系(图5,图6),第5列为当天第二次分装体系(图8),其中第1列和第5列对应孔位所加模板(重新抽提)一致(图7,图8),B6,D6,F6为同一批号不同批次分装试剂盒的弱阳性对照(图5),分别来自笔者分装试剂盒、当天第二次分装试剂盒、已检测为弱阳性的试剂盒。从上述结果可以看出,不同试剂盒中的弱阳性对照均有扩增,证明笔者分装试剂盒无质量问题,当天第二次分装试剂盒的弱阳性对照也无质量问题,结合图4扩增结果,图7、图8相同模板第1列有扩增而第5列无扩增,可以判定当天第二次分装的体系也存在问题。综上分析,同样的试剂盒,分装方法不同导致实验失败,大家将问题一致指向了分装时所使用的承装体系的透明小盖。难道是因为透明小盖上存在某种抑制物,抑制了PCR反应?图9 使用排枪给提取试剂预加蛋白酶K的透明小盖(容器) 图10使用排枪分装体系时混合扩增体系各成份的透明小盖(容器)由此,笔者逐一询问了前一天值班人员和当天值班人员提取试剂和扩增试剂准备的操作细节,发现前一天值班人员分装体系时误用了盛装蛋白酶K的专用透明小盖来盛装扩增体系,当天值班人员在进行复查时误用承装扩增体系的透明小盖来盛装蛋白酶K准备提取试剂。此时,失控原因终于有了眉头,也能很好的解释图1、图4和图8为什么扩增失败,尤其是当天第二次体系分装时虽然规范操作,但分装人员并不知情透明小盖已被蛋白酶K污染,以致最终实验失败。幸运的是当天第一次体系分装时专用透明小盖尚未被污染,分装的体系得以幸免。思路逐渐清晰,为了初步验证上述判断,笔者对已分装体系人为的进行了微量的蛋白酶K污染,看抑制效应能否再现,结果见图11、图12。为了进一步明确蛋白酶K的抑制效应和抑制浓度,笔者对蛋白酶K(原液浓度30mg/ml)进行95℃,10min灭活,同时对蛋白酶K的终浓度进行了梯度稀释,实验设计如表1。对上述不同干预浓度进行3个复孔扩增,模板为弱阳性对照(5ul/孔),扩增结果如下表2和图13-图20。
从上述结果我们可以看出,灭活后的蛋白酶K已不存在抑制效应(图17),进一步印证了实验失败的最重要的原因-蛋白酶K残留。从扩增曲线来看,终浓度5.689 mg/ml蛋白酶K可以完全抑制扩增反应(图13)。虽然低浓度的蛋白酶存在时(如低于0.5689mg/ml),从Ct值来看目的基因和内参基因基本不受影响(表2,图.18),但从扩增曲线对比来看,ORF1ab基因在终浓度0.5689mg/ml蛋白酶K存在时仍有显著的抑制效应,只是尚未能完全抑制扩增反应,N基因在终浓度0.005689mg/ml蛋白酶K存在时,扩增曲线 “指数期”较为平坦荧光强度较低,仍存在些许抑制效应,只是效应较小(图14、图15、图16、图17)。那么问题又来了,蛋白酶K到底是如何影响RT-PCR反应的呢?蛋白酶K(EC3.4.21.14)由一条肽链组成,包含277个氨基酸残基,相对分子质量为28.9kDa属丝氨酸蛋白酶类,蛋白酶K家族包含了各种真菌、酵母及革兰氏阴性细菌分泌的细胞内肽酶。1974年,Wolfgang Ebeling等利用沉淀、离子交换层析和凝聚层析等方法在林伯氏白色念球菌的培养基中分离纯化出蛋白酶K。因能合成该种蛋白酶的微生物能在以角蛋白(Keratin)为唯一碳氮源的环境中生长,即能够消化角蛋白,因此被命名为蛋白酶K。
与其它的蛋白酶相比较,蛋白酶K具有高活力和高稳定性,其酶活性不会被尿素、SDS和EDTA等变性剂抑制,且在高温、高盐或较高的pH等条件下,蛋白酶K仍能保持较高活性。因该酶在较广的pH范围(4~12.5)内及高温(50~70℃)均有活性,在提取DNA和RNA的缓冲液中具有很高的活性,可用于质粒或基因组DNA、RNA的分离,是DNA提取的关键试剂。在病毒核酸检测中,蛋白酶K是病毒采样液中的重要组分之一,蛋白酶K可以裂解病毒的外壳蛋白并使其失活,这样在运输和检测阶段更安全;另外,蛋白酶K还可以降解RNA酶,防止病毒RNA的降解,有利于核酸检测。
从扩增程序中我们不难发现,在逆转录阶段,温度设置为50℃且持续10min,而此阶段正好为蛋白酶K发挥效应提供了最适温度。由此判断,扩增体系中的逆转录酶和DNA 聚合酶均在此阶段遭受了不同程度的降解,从而出现了案例中出现的抑制效应。
通过此失控案例,笔者对日常质量控制和实验室管理进行了总结和反思:
PCR日常工作中,由于质控样品和标本同时检测同时出结果,一旦出现失控或结果异常,原因分析和复查将非常的耗时耗力,复查的平均时长少则持续80-90min,多则需要4-5h,如果中间再次出差错,将会造成严重的时间浪费。
本次失控原因查找过程中,通过观察反应曲线,虽然很快定位是前一天分装的体系出现问题,但未能明确是体系分装(体系混合盛装)的干扰,在后续复查中再次出现严重的操作污染,导致后续分装的体系扩增失败、附带弱阳性对照不出,造成了所有标本二次复查的窘境。不仅造成试剂的损耗和时间的浪费,差一点影响到失控原因的判断,所谓教训惨痛。因此,在PCR过程中,操作人员需要细心、细心、再细心,同时也提醒我们对日常的培训要深入细节,避免“细节性差错”重复发生。
在检验过程失控后,我们要学会去深挖失控背后的根本原因,不仅要知其然还要知其所以然。本案例中,通过查阅说明书,实验验证和回顾性分析,推断出蛋白酶K抑制扩增反应的关键步骤,最终明确了蛋白酶K抑制扩增反应的机制。虽然过程比较曲折,但为后续的工作积累了宝贵的经验。让“抑制物”这一概念有了非常深的认识,这将对后续的工作将起到非常深刻的警示作用。









































.jpg)